Estados Unidos ha rebasado las 20 millones de personas vacunadas contra el coronavirus, de las cuales más de 4.5 millones ya han recibido las dos dosis necesarias para tener una protección total contra la enfermedad.
Al 25 de enero, además de priorizar al personal de salud, la mayoría de los estados ya estaban administrando la vacuna a personas mayores de 65 y de 75 años, de acuerdo con información de la Kaiser Family Foundation.
[Siga las últimas noticias sobre la pandemia del coronavirus]
Hasta ahora, solo dos vacunas han sido autorizadas en Estados Unidos para su uso de emergencia: la de Moderna y la de Pfizer-BioNTech. Sin embargo, tres más se acercan a la solicitude de autorización de uso de emergencia en el país.
El presidente, Joe Biden, se ha comprometido a comprar 200 millones de dosis más para este verano, lo cual incrementaría a 600 millones el total de dosis de Pfizer-BioNTech y Moderna que estarán disponibles para los residentes de Estados Unidos.
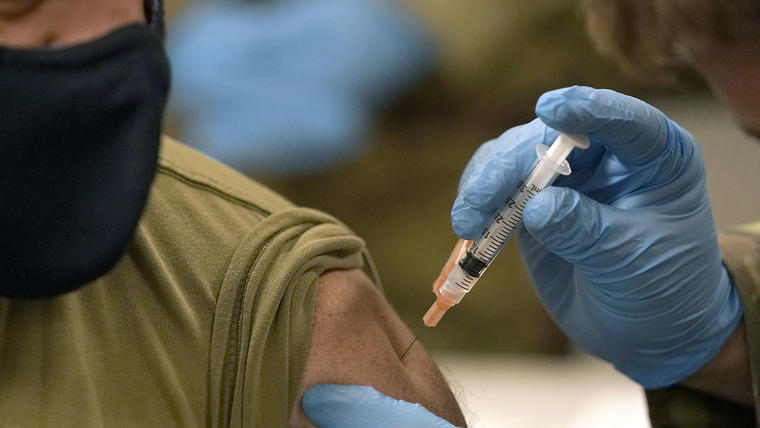
Es importante recordar que quienes obtengan la vacuna no pueden dejar de utilizar una mascarilla y respetar la distancia social. Seguir las recomendaciones de prevención ayudarán a las personas que aún no tienen la vacuna, y que siguen en riesgo de contraer el coronavirus.
Las vacunas que ya están siendo administradas en Estados Unidos:
✔️ Pfizer-BioNTech
La vacuna fue la primera en ser aprobada por la Administración de Alimentos y Medicamentos (FDA, en inglés) para su uso de emergencia en Estados Unidos, el pasado 11 de diciembre. Tiene una eficacia de 95% al prevenir el COVID-19 después de que se administran las dos dosis necesarias con una diferencia de 21 días.
Pfizer entregará 200 millones de dosis a Estados Unidos para finales de mayo, de acuerdo con Bloomberg.
[Cuáles son los efectos secundarios y qué tan seguras son las vacunas contra el coronavirus]
Los Centros de Control y Prevención de Enfermedades (CDC, en inglés) indican que la vacuna está recomendada para personas de 16 años y más. No está recomendada para personas que han tenido una reacción alérgica severa o inmediata al polietilengicol (PEG), uno de los ingredientes de la vacuna, o al polisorbato, que está relacionado con el PEG.
Efectos secundarios leves y moderados fueron comunes durante los ensayos clínicos, de acuerdo con los CDC. Efectos secundarios como fiebre, escalofríos, fatiga y dolor de cabeza son más comunes después de la segunda dosis de la vacuna.
✔️ Moderna
El 18 de diciembre, la FDA aprobó el uso de emergencia de la vacuna elaborada por Moderna. Esta vacuna necesita de dos dosis, administradas con 28 días de diferencia, para alcanzar una eficacia del 94.1% en la prevención de la enfermedad del COVID-19.
La compañía se ha comprometido a enviar 100 millones de dosis a Estados Unidos para finales de marzo, y 100 millones más en junio, de acuerdo con CNBC.
Los efectos secundarios más comunes de esta vacuna son dolor, inflamación y enrojecimiento en el área del brazo donde se recibió la inyección. También es común experimentar escalofríos, fatiga y dolor de cabeza.
Los CDC recomiendan que las personas de 18 años y más reciban esta vacuna. Al igual que la vacuna de Pfizer-BioNTech, no es recomendada para quienes tienen alergia al polietilengicol (PEG) o al polisorbato o para mujeres embarazadas.
Estas son las vacunas que han sido adquiridas para futura distribución, una vez obtengan la aprobación:
✔️ Johnson & Johnson
La farmacéutica Johnson & Johnson es la única desarrollando una vacuna de una sola dosis para el COVID-19. Este 29 de enero, la compañía anunció que está preparada para solicitar a la FDA la autorización de uso de emergencia en los Estados Unidos, lo que la podría convertir en la tercera vacuna autorizada en el país.
La vacuna fue efectiva para prevenir en 72% las infecciones moderadas y graves del coronavirus, así como en 85% los casos severos de la enfermedad. No obstante, su eficacia disminuyó a 57% en Sudáfrica, donde se ha detectado una variante con mayor transmisibilidad. En América Latina, la efectividad fue del 66%.
[El trastorno afectivo estacional aumentará este invierno debido a la pandemia]
Estas cifras son consideradas altas, en particular cuando se les compara con la efectividad del 40 a 60% de las vacunas contra la influenza, de acuerdo con The New York Times. El doctor Anthony Fauci, el principal infectólogo del país, explicó que el nivel de efectividad de la vacuna es suficiente para reducir las infecciones severas que acaban en hospitalización, reduciendo así la presión sobre el sistema de salud.
“Esta es la vacuna que puede marcar la diferencia con una sola dosis”, dijo el doctor Paul Stoffels, director científico de Johnson & Johnson.

De acuerdo con la farmacéutica, no se registraron reacciones alérgicas graves a la vacuna, y solo se documentaron efectos secundarios leves.
A diferencia de las vacunas de Pfizer-BioNTech y Moderna, que se basan en tecnología genética llamada ARNm, esta vacuna usa un adenovirus modificado, el cual provoca resfriados comunes, para llevar instrucciones a las células del cuerpo e impulsar una respuesta inmunológica, de acuerdo con CNN.
✔️ Oxford - AstraZeneca
Un ensayo clínico con más de 5,800 voluntarios en Reino Unido, Sudáfrica y Brasil concluyó que las dos dosis de esta vacuna tienen una efectividad del 62% para prevenir infecciones sintomáticas del COVID-19.
La FDA no ha recibido la información sobre esa tercera fase del ensayo clínico, necesaria para autorizar su uso de emergencia. En cambio, la farmacéutica espera los resultados de un ensayo clínico realizado en Estados Unidos con 30,000 participantes, de acuerdo con Business Insider.
[¿Por qué están apareciendo ahora nuevas variantes del coronavirus?]
Los resultados serán dados a conocer hasta que 75% de los participantes en el estudio se hayan contagiado del virus, y al menos dos meses hayan pasado desde la aplicación de la vacuna, a fin de evaluar su seguridad.
La institución reguladora de la Unión Europea recomendó autorizar la vacuna de Oxford-AstraZeneca el 29 de enero, aunque no hay información suficiente sobre su eficacia en adultos mayores, quienes solo representaron el 6% de los participantes en los ensayos clínico, según The Washington Post.
✔️ Novavax
Esta vacuna tiene una efectividad del 89.3% para prevenir el COVID-19, según informó la compañía esta semana con base en un ensayo realizado con 15,000 personas en el Reino Unido. Sin embargo, en un pequeño ensayo realizado en Sudáfrica, la efectividad bajo a menos de 50%.
Esta pequeña compañía fue una de las seis que recibió recursos federales como parte del Operación Warp Speed, a fin de desarrollar una vacuna contra el coronavirus. Actualmente lleva a cabo la fase 3 de sus ensayos clínicos en Estados Unidos y México, para evaluar la seguridad y efectividad de la vacuna en 30,000 personas de 18 años y más.
Esta vacuna inyecta proteínas de coronavirus sintetizadas para reactivar el sistema inmunológico del cuerpo.
Con información de KFF, Bloomberg, CNBC, The New York Times, CNN, Business Insider, The Washington Post